מחקרים מראים כי מקרופאגים אינטרסטיציאליים הם באופן בלתי צפוי המטרה העיקרית של SARS-CoV-2 בריאות, מה שמוביל ל-COVID-19 חמור, מה שמצביע על מטרות טיפוליות חדשות. קרדיט: twoday.co.il.com
סוג של תא חיסון שהתעלם ממנו בעבר מאפשר SARS-CoV-2 להתרבות, מצאו מדעני סטנפורד רפואה. לגילוי יש השלכות חשובות למניעת חמורים COVID 19.
סוג תאי הריאה הרגיש ביותר לזיהום על ידי SARS-CoV-2, ה נגיף שגורם ל-COVID-19, אינו זה שהניח בעבר כפגיע ביותר. יתרה מכך, הנגיף חודר לתא הרגיש הזה במסלול לא צפוי. ההשלכות הרפואיות עשויות להיות משמעותיות.
חוקרי רפואת סטנפורד הטילו סוג של תא חיסון המכונה מקרופאג אינטרסטיציאלי במעבר הקריטי ממקרה מטריד בלבד של COVID-19 למקרה שעלול להיות קטלני. מקרופאגים אינטרסטיציאליים ממוקמים עמוק בתוך הריאות, ומגנים בדרך כלל על האיבר היקר הזה על ידי, בין היתר, ספוג וירוסים, חיידקים, פטריות וחלקיקי אבק שעושים את דרכם בדרכי הנשימה שלנו. אבל זה בדיוק התאים האלה, הראו החוקרים במחקר שפורסם ב-10 באפריל ב- כתב עת לרפואה ניסיוניתשמכל סוגי התאים המוכרים המרכיבים רקמת ריאה הם הרגישים ביותר לזיהום על ידי SARS-CoV-2.
המדענים למדו כי מקרופאגים ביניים נגועים ב-SARS-CoV-2, הופכים ליצרני וירוסים ומשפריצים אותות כימיים דלקתיים ומעוררי רקמות צלקות, מה שעלול לסלול את הדרך לדלקת ריאות ולגרום נזק לריאות עד לנקודה שבה הנגיף, לאורך עם אותם חומרים חזקים המופרשים, יכול לפרוץ מהריאות ולחולל הרס בכל הגוף.
הממצאים המפתיעים מצביעים על גישות חדשות במניעת זיהום SARS-CoV-2 מלהפוך למחלה מסכנת חיים. אכן, הם עשויים להסביר מדוע נוגדנים חד שבטיים שנועדו להילחם ב-COVID הקשה לא פעלו טוב, אם בכלל – וכאשר הם כן עבדו, זה היה רק כאשר הם ניתנו מוקדם במהלך ההדבקה, כאשר הנגיף הדביק תאים ב דרכי הנשימה העליונות המובילות לריאות, אך עדיין לא התגבשו ברקמת הריאה.
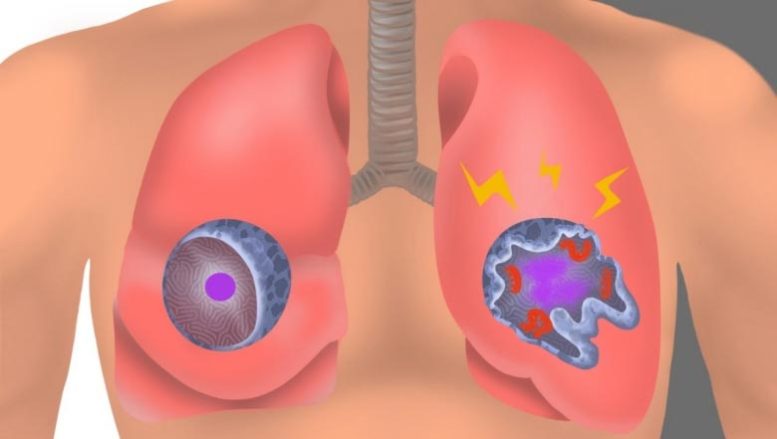
במקרופאג אינטרסטיציאלי לא נגוע, הגרעין (סגול) וקרום התא החיצוני (כחול) שלמים. במקרופאג אינטרסטיציאלי נגוע, הגרעין מנותץ, רכיבים ויראליים רבים (אדומים) מתקבצים יחדיו, והתא משדר אותות כימיים דלקתיים ומעוררי רקמות צלקות (צהוב). קרדיט: אמילי מוסקל
הווירוס מפתיע
"הבטלנו מספר הנחות שווא לגבי האופן שבו הנגיף באמת משתכפל בריאה האנושית", אמרה קתרין בליש, MD, PhD, פרופסור למחלות זיהומיות ולמיקרוביולוגיה ואימונולוגיה והפרופסורים של ג'ורג' א. ולוסי בקר ב- רפואה ודיקן עמית למחקר בסיסי ותרגומי.
בליש הוא המחבר הבכיר של המחקר, יחד עם מארק קרסנוב, MD, PhD, הפרופסור לביוכימיה של פול ומילדרד ברג והמנהלת של מרכז ורה מולטון וול למחלות כלי דם ריאתיות.
"השלב הקריטי, לדעתנו, הוא כאשר הנגיף מדביק מקרופאגים אינטרסטיציאליים, ומעורר תגובה דלקתית מסיבית שיכולה להציף את הריאות ולהפיץ זיהום ודלקת לאיברים אחרים", אמר קרסנוב. חסימת הצעד הזה, לדבריו, עשויה להתגלות כהתקדמות טיפולית גדולה. אבל יש תפנית בעלילה: לוירוס יש דרך יוצאת דופן להיכנס לתוך התאים האלה – דרך שמפתחי תרופות עדיין לא למדו כיצד לחסום ביעילות – המחייבת התמקדות חדשה במנגנון האלטרנטיבי הזה, הוא הוסיף.
במאמר שפורסם ב טֶבַע בתחילת 2020, קרסנוב ועמיתיו, כולל הסטודנט לתואר שני, קייל טרוואגליני, דוקטורט – שהוא גם אחד מהמחברים המובילים במחקר החדש יחד עם סטודנט ל-MD-PhD טימותי וו – תיארו טכניקה שהם פיתחו לבידוד טריים ריאות אנושיות; ניתוק התאים זה מזה; ואפיון אותם, אחד אחד, על סמך אילו גנים בתוך כל תא היו פעילים ועד כמה. באמצעות טכניקה זו, מעבדת קרסנוב ומשתפי הפעולה הצליחו להבחין ביותר מ-50 סוגי תאים שונים, והרכיבו אטלס של תאי ריאה בריאים.
"רק ריכזנו את האטלס הזה כשמגיפת COVID-19 פגעה", אמר קרסנוב. זמן קצר לאחר מכן, נודע לו שבליש וארג'ון רוסטאגי, MD, PhD, מדריך למחלות זיהומיות ומחבר מוביל נוסף של המחקר, בונים מתקן אולטרה בטוח שבו יוכלו לגדל בבטחה SARS-CoV-2 ולהדביק תאים עם זה.
נוצר שיתוף פעולה. קרסנוב ובליש ושותפיהם השיגו רקמת ריאה בריאה טרייה שנכרתה משבעה חולים כירורגיים וחמישה תורמי ריאות שנפטרו שריאותיהם היו נקיות מנגיפים אך מסיבה זו או אחרת לא השתמשו בהשתלות. לאחר שהדביקו את רקמת הריאה ב-SARS-CoV-2 והמתינו יום עד שלושה ימים להתפשטות הזיהום, הם הפרידו והקלידו את התאים כדי ליצור אטלס תאי ריאה נגועים, מקביל לזה שהצוות של קרסנוב יצר עם ריאה בריאה תאים. הם ראו את רוב סוגי התאים שהצוות של קרסנוב זיהה ברקמת ריאה בריאה.
כעת המדענים יכלו להשוות תאי ריאות בתוליים לעומת תאי ריאות נגועים ב-SARS-CoV-2 מאותו סוג תאים ולראות כיצד הם שונים: הם רצו לדעת אילו תאים הנגיף נגוע, באיזו קלות SARS-CoV-2 משתכפל בתאים נגועים, ו אילו גנים התאים הנגועים הגדילו או הצביעו למטה בהשוואה לרמות הפעילות של עמיתיהם הבריאים. הם הצליחו לעשות זאת עבור כל אחד מעשרות סוגי התאים השונים שהם זיהו גם בריאות בריאות וגם נגועות.
"זה היה ניסוי פשוט, והשאלות ששאלנו היו ברורות", אמר קרסנוב. "זה היה ה תשובות לא היינו מוכנים".
ההנחה היא שהתאים בריאות הפגיעים ביותר לזיהום SARS-CoV-2 הם אלה הידועים כתאים מכתשית מסוג 2. הסיבה לכך היא שהמשטחים של תאים אלה, יחד עם אלו של סוגי תאים רבים אחרים בלב, במעיים ובאיברים אחרים, מכילים עותקים רבים של מולקולה המכונה ACE2. הוכח כי SARS-CoV-2 מסוגל לתפוס את ACE2 ולתמרן אותו בצורה שתאפשר לנגיף לתמרן את דרכו לתוך התאים.
תאי Alveolar Type 2 פגיעים במידה מסוימת ל-SARS-CoV-2, כך גילו המדענים. אבל סוגי התאים שהיו ללא ספק הנגועים בתדירות הגבוהה ביותר התבררו כשני זנים של סוג תאים שנקרא מקרופאג.
מפעלי וירוסים
המילה "מקרופאג" מגיעה משני מונחים יווניים שפירושם, בערך, "אוכל גדול". השם הזה לא זכה. האוויר שאנו שואפים נושא לא רק חמצן אלא, למרבה הצער, חלקיקי לכלוך זעירים הנישאים באוויר, נבגי פטריות, חיידקים ווירוסים. מקרופאג מרוויח את החזקתו, בין היתר, בזלילת הגופים הזרים הללו.
דרכי הנשימה המובילות לריאות שלנו מגיעות לשיא באינספור alveoli, שקי אוויר זעירים בעובי תא אחד, אשר ניגשות אליהם נימים בשפע. ממשק זה, הנקרא interstitium, הוא המקום שבו חמצן באוויר שאנו נושמים נכנס לזרם הדם ולאחר מכן מופץ לשאר הגוף על ידי מערכת הדם.
שני סוגי המקרופאגים הקשורים ל-SARS-CoV-2 הרגישים לריאות ממוקמים בשני מקומות שונים. מה שנקרא מקרופאגים alveolar מסתובבים בחללי האוויר בתוך alveoli. לאחר ההידבקות, התאים הללו מבעבעים, מייצרים ומטפטפים צאצאים ויראליים בקצב מזדמן, אך פחות או יותר שומרים על שפה עליונה נוקשה ושומרים על תפקודם הרגיל. התנהגות זו עשויה לאפשר להם להזין את ההתקדמות של SARS-CoV-2 על ידי דגירה ויצירת אספקה קבועה של חלקיקים ויראליים חדשים שנמלטים בהתגנבות וחודרים לשכבת התאים העוטפת את המכתשות.
מקרופאגים אינטרסטיציאליים, סוג התאים האחר שהתגלה כנגוע בקלות ובעומק על ידי SARS-CoV-2, מפטרלים בצד הרחוק של המכתשים, שם גומי החמצן פוגש את הדרך של כדוריות הדם האדומות. אם חלקיק ויראלי פולש או חיידק אחר מצליח להתחמק מהערנות של מקרופאגים מכתשית, להדביק ולחבור דרך שכבת התאים העוטפת את המכתשית, ולסכן לא רק את הריאות אלא את שאר הגוף, מקרופאגים בין-תאי מוכנים לקפוץ פנימה ולהגן על שְׁכוּנָה.
לפחות, בדרך כלל. אבל כשמקרופאג ביניים פוגש את SARS-CoV-2, זה סיפור אחר. במקום להיאכל על ידי התא החיסוני אוכל הכל, הנגיף מדביק אותו.
ומקרופאג ביניים נגוע לא סתם מעשן; זה עולה באש. כל הגיהנום משתחרר כשהנגיף ממש תופס את השליטה ומשתלט, חוטף את החלבון והגרעין של התא.חוּמצָה-מכונות לייצור. במהלך הפקת מספר עצום של עותקים של עצמו, SARS-CoV-2 הורס את הגבולות המפרידים בין גרעין התא משאר התא כמו מרית המתנפצת ומפזרת את החלמון של ביצה גולמית. הצאצאים הנגיפיים יוצאים מהמקרופאג המושקע ועוברים להדביק תאים אחרים.
אבל זה לא הכל. בניגוד למקרופאגים מכתשיים, מקרופאגים בינ-סטיציאליים נגועים שואבים חומרים שמאותתים לתאי חיסון אחרים במקומות אחרים בגוף ללכת לריאות. אצל מטופל, הציע קרסנוב, זה יעורר זרימה דלקתית של תאים כאלה. כאשר הריאות מתמלאות בתאים ובנוזל שמגיע איתן, חילופי החמצן הופכים לבלתי אפשריים. המחסום השומר על שלמות המכתשית ניזוק בהדרגה. דליפה של נוזלים נגועים ממכתשות פגומות דוחפת צאצאים ויראליים לזרם הדם, ומפיצה את הזיהום והדלקת לאיברים מרוחקים.
עם זאת, חומרים אחרים המשתחררים על ידי מקרופאגים בין-סטיציאליים נגועים ב-SARS-CoV-2 מעוררים את הייצור של חומר סיבי ברקמת החיבור, וכתוצאה מכך צלקות של הריאות. בחולה חי, החלפת תאים חדורי חמצן ברקמת צלקת תגרום לריאות להיות בלתי מסוגלות לבצע חילופי חמצן.
"אנחנו לא יכולים לומר שתא ריאה שיושב בצלחת הולך לחלות ב-COVID," אמר בליש. "אבל אנחנו חושדים שזו הנקודה שבה, בחולה בפועל, הזיהום עובר מניהול לחמור."
עוד נקודת כניסה
המרכיב את הממצא הבלתי צפוי הזה הוא הגילוי ש-SARS-CoV-2 משתמש בנתיב שונה להדבקת מקרופאגים אינטרסטיציאליים מזה שבו הוא משתמש כדי להדביק את הסוגים האחרים.
שלא כמו תאי מכתשית מסוג 2 ומקרופאגים מכתשיים, שאליהם הנגיף מקבל גישה על ידי היצמדות ל-ACE2 על פני השטח שלהם, SARS-CoV-2 מתפרץ למקרופאגים אינטרסטיציאליים באמצעות קולטן שונה שהתאים הללו מציגים. במחקר, חסימת הקישור של SARS-CoV-2 ל-ACE2 הגנה על התאים הראשונים, אך לא הצליחה לפגוע ברגישותם של התאים האחרונים לזיהום ב-SARS-CoV-2.
"SARS-CoV2 לא השתמש ב-ACE2 כדי להיכנס למקרופאגים אינטרסטיציאליים", אמר קרסנוב. "זה נכנס דרך קולטן אחר בשם CD209."
נראה כי זה מסביר מדוע נוגדנים חד שבטיים שפותחו במיוחד כדי לחסום את האינטראקציה של SARS-CoV-2/ACE2 לא הצליחו להפחית או למנוע מקרים חמורים של COVID-19.
הגיע הזמן למצוא סט חדש לגמרי של תרופות שיכולות לעכב את הקישור של SARS-CoV-2/CD209. עכשיו, אמר קרסנוב.
המחקר מומן על ידי ה המכונים הלאומיים לבריאות (מעניקה K08AI163369, T32AI007502 ו-T32DK007217), קרן ביל ומלינדה גייטס, צ'אן צוקרברג ביוהוב, קרן Burroughs Wellcome, Stanford Chem-H, מאיץ הרפואה החדשנית של סטנפורד והמכון הרפואי הווארד יוז.