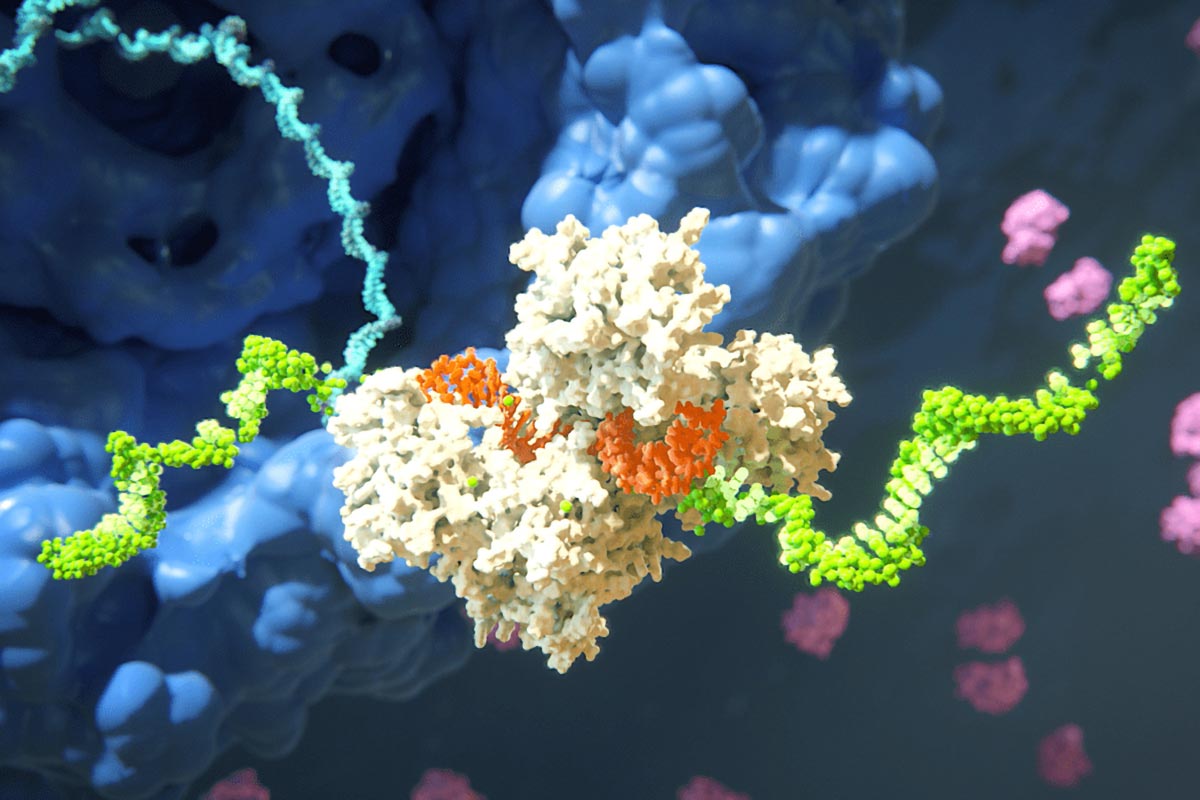
Alnylam Pharmaceuticals מתרגמת את ההבטחה למחקר הפרעות RNA (RNAi) לסוג חדש של טיפולים רבי עוצמה מבוססי גנים. בעיבוד זה, הגדיל הירוק הוא ה-mRNA הממוקד, והאובייקט הלבן הוא ה-RNA-induced silencing complex (RISC) שיכול למנוע את הביטוי של חלבוני ה-mRNA של המטרה. הגדיל הכתום הוא RNAi. קרדיט: באדיבות אלנילם פרמצבטיקה
המסע מגילוי מחקר לטיפולים חדשים בעלי השפעה
אלנילם פרמצבטיקה, נוסדה על ידי MIT פרופסורים ופוסט-דוקטורנטים לשעבר, פיתחה חמש תרופות RNAi שאושרו על ידי ה-FDA, שהשפיעו באופן משמעותי על חיי המטופלים. החברה ממשיכה לחדש באספקת RNAi, במטרה לטפל במחלות שונות, כולל הפרעות נוירולוגיות.
לפני שתגלית מחקרית הופכת לטיפול משנה חיים עבור מטופלים, יש הרבה מכשולים שצריך לפנות. זה נכון במיוחד כאשר הטיפולים המפותחים מייצגים סוג חדש לגמרי של תרופות. עם זאת, התגברות על המכשולים הללו יכולה לחולל מהפכה ביכולת שלנו לטפל במחלות.
חברות מעטות מדגימות את התהליך הזה טוב יותר מאלנילם פרמצבטיקה. אלנילם הוקמה על ידי קבוצה של חוקרים הקשורים ל-MIT שהאמינו בהבטחה של טכנולוגיה – RNA הפרעה, או RNAi.
ייסוד ופיתוח מוקדם
החוקרים עשו עבודה בסיסית כדי להבין כיצד RNAi, שהוא תהליך המתרחש באופן טבעי, פועל להשתיק גנים באמצעות השפלה של RNA שליח. אבל החלטתם להקים את אלנילם ב-2002 היא שמשכה את המימון והמומחיות הדרושים כדי להפוך את התגליות שלהם לסוג חדש של תרופות. מאז ההחלטה ההיא, אלנילם עשתה התקדמות יוצאת דופן ולקחה את RNAi מתגלית מדעית מעניינת למסלול טיפול חדש ומשפיע.
כיום יש לאלנילם חמש תרופות שאושרו על ידי מינהל המזון והתרופות האמריקאי (תרופת RNAi אחת שהתגלתה על ידי אלנילם מורשית לנוברטיס) וצנרת קלינית המתרחבת במהירות. התרופות המאושרות של החברה מיועדות למצבים מתישים, לפעמים קטלניים, שמטופלים רבים התמודדו איתם במשך עשרות שנים עם מעט אפשרויות אחרות.
החברה מעריכה שהטיפולים שלה עזרו ליותר מ-5,000 חולים בשנת 2023 בלבד. מאחורי המספר הזה עומדים סיפורי סבלנות שממחישים כיצד אלנילם שינתה חיים. אם לשלושה ילדים אומרת שהטיפולים של אלנילם עזרו לה להחזיר את השליטה על חייה לאחר שהייתה מרותקת למיטה עם התקפים הקשורים למחלה הגנטית הנדירה החריפה פורפיריה לסירוגין (AIP). מטופלת אחרת דיווחה שאחד מהטיפולים של החברה עזר לה להגיע לחתונה של בתה. מטופל שלישי, שעזב את הקולג' עקב התקפות AIP תכופות, הצליח לחזור לבית הספר.
כיום אלנילם אינה החברה היחידה המפתחת תרופות מבוססות RNAi. אבל היא עדיין חלוצה בתחום, ומייסדי החברה – פרופסור פיל שארפ במכון MIT, פרופסור דיוויד ברטל, פרופסור אמריטוס פול שימל, והפוסט-דוקטורנטים לשעבר של MIT תומאס טושל ופיליפ זמור – רואים באלנילם אלוף בתחום באופן רחב יותר. .
"אלנילם פרסמה יותר מ-250 מאמרים מדעיים במשך 20 שנה", אומר שארפ, המכהן כיום כיו"ר הוועדה המייעצת המדעית של אלנילם. "לא רק עשינו את המדע, לא רק שתרגמנו אותו לטובת המטופלים, אלא גם תיארנו כל שלב. הקמנו את זה כדרך לטיפול בחולים, ואני מאוד גאה בשיא הזה".
פיתוח RNAi חלוצי
מעורבותה של MIT ב-RNAi מתחילה מגילויה. לפני שאנדרו פייר PhD '83 חלק פרס נובל על גילוי RNAi בשנת 1998, הוא עבד על הבנת איך DNA הועתק ל-RNA, כסטודנט לתואר שני במעבדה של שארפ.
לאחר שעזב את MIT, Fire ומשתפי פעולה הראו שניתן להשתמש ב-RNA דו-גדילי כדי להשתיק גנים ספציפיים בתולעים. אבל המנגנונים הביוכימיים שאפשרו ל-RNA דו-גדילי לעבוד לא היו ידועים עד שהפרופסורים של MIT שארפ, ברטל ורות להמן, יחד עם זמור וטושל, פרסמו מאמרים בסיסיים שהסבירו את התהליך. החוקרים פיתחו מערכת לחקר RNAi והראו כיצד ניתן לשלוט ב-RNAi באמצעות רצפים גנטיים שונים. זמן קצר לאחר שטושל עזב את MIT, הוא הראה שניתן להשתמש בתהליך דומה גם כדי להשתיק גנים ספציפיים בתאים אנושיים, ולפתוח גבול חדש בחקר הגנים ובסופו של דבר בטיפול במחלות.
תגליות טרנספורמטיביות
"תום הראה שאתה יכול לסנתז את הרנ"א הקטנים האלה, להמיר אותם לתאים, ולקבל הרס ספציפי מאוד של הגן שתואם לזה של הרנ"א הקטנים", מסביר ברטל. "הגילוי הזה שינה את המחקר הביולוגי. היכולת להפיל באופן ספציפי גן של יונקים הייתה עצומה. אתה יכול לפתע לחקור את התפקוד של כל גן שאתה מעוניין בו על ידי הפלתו ולראות מה קורה. קהילת המחקר החלה מיד להשתמש בגישה זו כדי לחקור את תפקוד הגנים האהובים עליהם בתאי יונקים."
מעבר להארת תפקוד הגנים, עלתה בראש יישום נוסף.
"מכיוון שכמעט כל המחלות קשורות לגנים, האם נוכל לקחת את ה-RNA הקטנים האלה ולהשתיק גנים כדי לטפל בחולים?" שארפ זוכרת שתהה.
כדי לענות על השאלה, החוקרים הקימו את אלנילם בשנת 2002. (הם גייסו את שימל, מוותיקי ביוטק, בערך באותו זמן.) אבל הייתה עבודה רבה לפני שניתן היה לנסות את הטכנולוגיה בחולים. האתגר העיקרי היה הכנסת RNAi לציטופלזמה של תאי החולים.
"באמצעות עבודה במעבדה של דייב ברטל ופיל שארפ, בין היתר, התברר שכדי להפוך RNAi לטיפולים, יש שלוש בעיות לפתור: לידה, לידה ולידה", אומר קצין המדעי הראשי של אלנילם, קווין פיצג'רלד, שהיה עם החברה מאז 2005.
בשלב מוקדם, אלנילם שיתף פעולה עם מומחה למתן תרופות מ-MIT ופרופסור המכון בוב לנגר. בסופו של דבר, אלנילם פיתחה את ננו-חלקיקי השומנים הראשונים (LNPs) שניתן להשתמש בהם כדי לעטוף RNA ולהעביר אותו לתאי המטופל. LNPs שימשו מאוחר יותר בחיסוני mRNA עבור Covid-19.
"אלנילם השקיעה למעלה מ-20 שנה ויותר מ-4 מיליארד דולר ב-RNAi כדי לפתח את הטיפולים החדשים הללו", אומר שארפ. "זה האמצעי שבאמצעותו ניתן לתרגם חידושים לטובת החברה."
מפריצת דרך מדעית ועד ליד מיטת החולה
אלנילם קיבלה את אישור ה-FDA הראשון שלה ב-2018 לטיפול בפולינוירופתיה של עמילואידוזיס תורשתית בתיווך טרנסטירטין, מחלה נדירה וקטלנית. זה שימש כטיפול ה-RNAi הראשון שהגיע לשוק והתרופה הראשונה שאושרה לטיפול במצב זה בארצות הברית.
"מה שאני זוכר זה שבסופו של יום עבור חולים מסוימים, חודשיים זה הכל", אומר פיצג'רלד. "המחלות שאנו מנסים לטפל בהן מתקדמות חודש אחר חודש, מיום ליום, והחולים יכולים להגיע לנקודה שבה שום דבר לא עוזר להם. אם אתה יכול להעביר את המחלה שלהם בשלב, זה עצום".
מאז אותו טיפול ראשון, אלנילם עדכנה את מערכת אספקת ה-RNAi שלה – כולל על ידי צימוד RNA מפריעים קטנים למולקולות שעוזרות להם להיכנס לתאים – וזכתה באישורים לטיפול במחלות גנטיות נדירות אחרות יחד עם כולסטרול גבוה (הטיפול המורשה לנוברטיס). כל הטיפולים הללו פועלים בעיקר על ידי השתקת גנים המקודדים לייצור חלבונים בכבד, שהוכח כמקום הקל ביותר להעברת מולקולות RNAi. אבל הצוות של אלנילם בטוח שהם יכולים להעביר RNAi לאזורים אחרים בגוף, מה שיפתח עולם חדש של אפשרויות טיפול. החברה דיווחה על תוצאות מוקדמות מבטיחות במערכת העצבים המרכזית ואומרת שמחקר שלב ראשון בשנה שעברה היה הטיפול הראשון ב-RNAi שהדגים השתקת גנים במוח האנושי.
סיכויי עתיד ויעדים
"יש הרבה עבודה שנעשית באלנילם ובחברות אחרות כדי לספק את ה-RNAis האלה לרקמות אחרות: שרירים, תאי חיסון, תאי ריאה וכו'", אומר שארפ. "אבל בעיני האפליקציה המעניינת ביותר היא משלוח למוח. אנו חושבים שיש לנו שיטת טיפול שיכולה לשלוט באופן ספציפי מאוד בפעילות של גנים מסוימים במערכת העצבים. אני חושב שזה חשוב בצורה יוצאת דופן, למחלות מ אלצהיימר לסכיזופרניה ודיכאון".
עבודת מערכת העצבים המרכזית משמעותית במיוחד עבור פיצג'רלד, שצפה באביו נאבק בפרקינסון.
"המטרה שלנו היא להיות בכל איבר בגוף האדם, ואז שילובים של איברים, ואז שילובים של מטרות בתוך איברים בודדים, ואז שילובים של מטרות בתוך ריבוי איברים", אומר פיצג'רלד. "אנחנו ממש בתחילת הדרך של מה שהטכנולוגיה הזו תעשה לבריאות האדם."
זו תקופה מרגשת עבור הקהילה המדעית של RNAi, כולל רבים שממשיכים ללמוד אותה ב-MIT. ובכל זאת, אלנילם תצטרך להמשיך ולבצע את מאמצי פיתוח התרופות שלה כדי לקיים את ההבטחה הזו ולעזור למאגר מתרחב של חולים.
"אני חושב שזה גבול אמיתי", אומר שארפ. "יש צורך טיפולי גדול, ואני חושב שלטכנולוגיה הזו יכולה להיות השפעה עצומה. אבל אנחנו צריכים להוכיח את זה. לכן אלנילם קיים: לעסוק במדע חדש שפותח אפשרויות חדשות ולגלות אם אפשר לגרום להן לעבוד. זו, כמובן, גם הסיבה ש-MIT כאן: לשפר חיים".