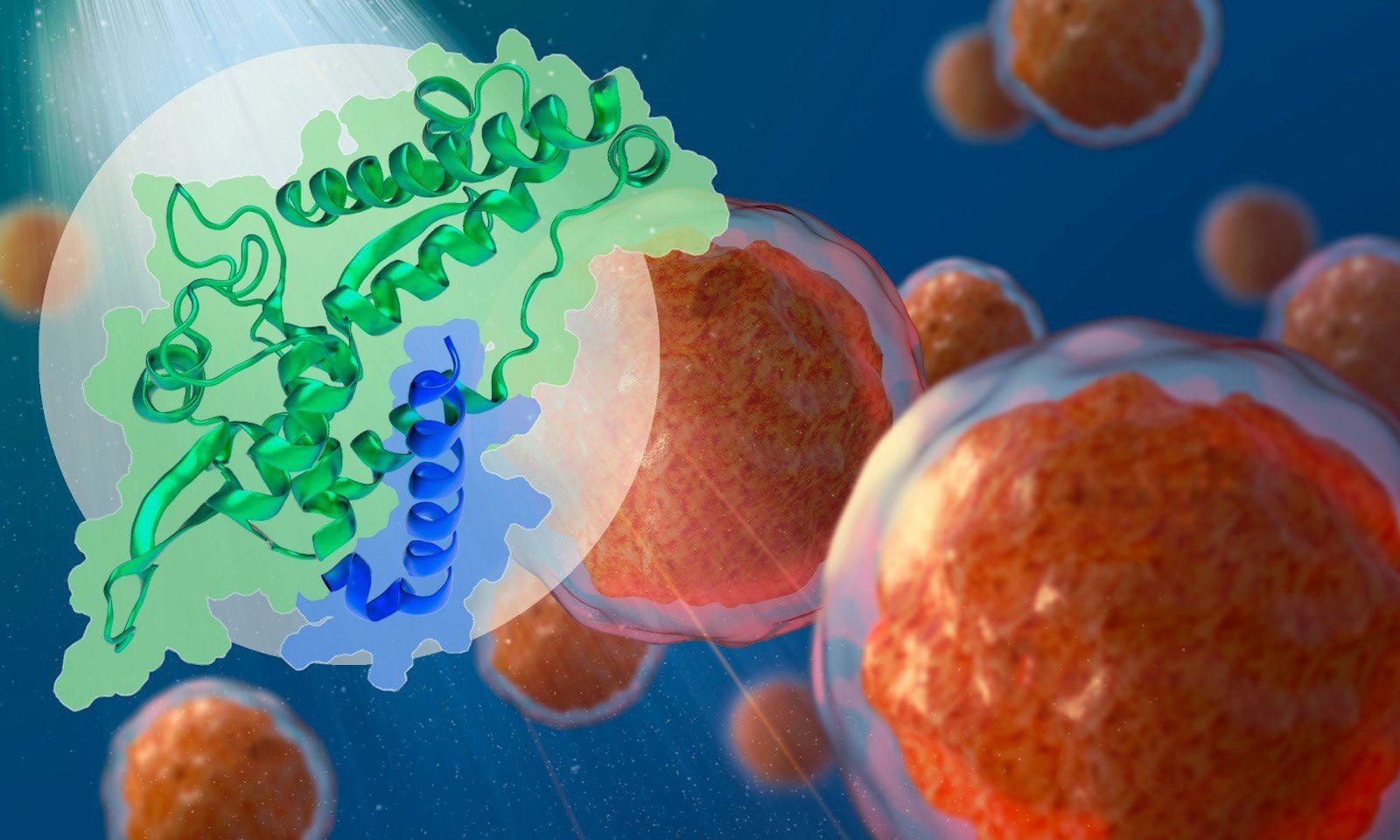
המחקר החדש מדגים את הבסיס המבני של האינטראקציה בין חלבונים מעודדי סרטן MAGEA4 (ירוק) ו-RAD18 (כחול). קרדיט: איזבל רומרו קלבו/EMBL
מחקר שנערך לאחרונה על ידי קבוצת Bhogaraju ב-EMBL Grenoble חשף את המנגנונים שבאמצעותם משפחת חלבוני MAGE, הידועה בתפקידם בקידום הסרטן, מתחברת למטרותיהם. תגלית זו סוללת את הדרך ליצירת תרופות אנטי-סרטניות שתוכננו במיוחד לעכב חלבונים אלו.
חוקרים ב-EMBL Grenoble, בראשות קבוצת Bhogaraju, גילו דרכים חדשות שבהן משפחת חלבונים הקשורה לסרטן קושרת את מטרותיהן. תוצאות המחקר, שפורסמו ב כתב העת EMBOעשוי לסייע בפיתוח תרופות נגד סוגי סרטן מסוימים עמידים לכימותרפיה והקרנות.
משפחת מלנומה אנטיגן גן (MAGE) מורכבת מיותר מ-40 חלבונים בבני אדם, שרובם נמצאים באשכים רק בתנאים בריאים. עם זאת, בסוגי סרטן רבים, חלבונים אלו נמצאים ברמות גבוהות ברקמות שבהן הם אינם מתבטאים בדרך כלל ומאמינים כי הם ממלאים תפקיד בקידום התקדמות הסרטן.
חלבון MAGE אחד כזה – MAGEA4 – ידוע באינטראקציה עם RAD18, חלבון שידוע שיש בשפע בחלק מהתאים הסרטניים. האחרון הוא חלק מהמנגנון המולקולרי שעוזר לתא לתקן את הנזק שלו DNA. רמות גבוהות של RAD18 אחראיות לעמידות של מספר סוגי סרטן לכימותרפיה גנוטוקסית (מזיקה ל-DNA).
תפקידו של RAD18 בהתנגדות לתאי סרטן
RAD18 מתפקד על ידי הצמדת תגים מולקולריים קטנים – הנקראים יוביקוויטין – לחלבונים שונים. תג זה, כמו בול דואר, אומר לתא מה יהיה גורלו של החלבון הזה. RAD18 יכול גם לצרף את התג הזה לעצמו – תהליך הנקרא אוטווביקוויטינציה. זה מכוון אותו לפירוק, כלומר אומר לתא להיפטר מרמות עודפות של חלבון זה.
קבוצת Bhogaraju ב-EMBL Grenoble משתמשת בגישות מבוססות מבניות וביולוגיה של תאים כדי לחקור מסלולים מבוססי אוביקוויטין כאלה בפיזיולוגיה ומחלות נורמליות. הצוות, בשיתוף עם קבוצת הניג ב-EMBL היידלברג, החליט לבחון לעומק את האינטראקציה בין החלבונים MAGEA4 ו-RAD18, באמצעות AlphaFoldכלי מבוסס בינה מלאכותית המאפשר למדענים לחזות את מבנה החלבונים.
הצוות, שכלל את הדוקטורנטית של קבוצת Bhogaraju, Simonne Griffith-Jones והפוסט-דוקטורט Urbi Mukhopadhyay, גילה של-MAGEA4 יש חריץ שיכול לקשור חלק מהחלבון RAD18, מה שמונע מהאחרון להצמיד לעצמו קבוצות יוביקוויטין ולאחר מכן להתפרק.
מעניין שהחוקרים יכלו להשתמש במקטע חלבון סינתטי קצר, המחקה את החלק של RAD18 הקושר את החריץ ב-MAGEA4, כדי לחסום את האינטראקציה בין שני החלבונים. זה עשוי לסלול את הדרך לתכנון של תרופות המכוונות למתחם זה ולמנוע הצטברות RAD18 בתוך תאים סרטניים.
החוקרים מצאו גם חריץ דומה מאוד בחלבון אחר ממשפחת MAGE, המשמש לוויסות חלבון אחר המעודד סרטן. הם מאמינים שהחריץ הזה עשוי להיות תכונה כללית של משפחת MAGE, המשמשת לתווך קישור לחלבונים רלוונטיים לסרטן.
בנוסף לחריץ, המדענים גם הבחינו ששני חלקים בחלבון RAD18 מקיימים אינטראקציה זה עם זה, מה שעוזר לו לחבר את תג האוביקוויטין לחלבון שמקדם את הישרדות תאי הסרטן. הם יכולים לחסום את הפונקציה הזו באמצעות אסטרטגיות גנטיות, מה שמרמז שתרופות עתידיות שנועדו לחסום אינטראקציה זו עלולות לגרום לרגישות מחדש לתאים סרטניים שצברו עמידות לכימותרפיה או לקרינה.
"אנו נרגשים מהנתונים הללו מכיוון שנראה שהממצאים שלנו ישימים ל-MAGEs רבים שפותחים שער למיקוד ב-MAGEs המניעים סרטן", אמר Sagar Bhogaraju, ראש קבוצה ב-EMBL Grenoble. "אנחנו עובדים כעת על פיתוח שיטות לסינון תרכובות אשר לאגד את הנקודה החמה שהתגלתה לאחרונה של MAGEs."