חוקרי MIT השתמשו בפרופיל RNA חד-תא כדי לחקור שינויים בביטוי הגנים במוחם של חולי אלצהיימר, תוך התמקדות בפגיעויות נוירונאליות ובגורמים לחוסן קוגניטיבי. המחקר הדגיש את ההשפעה המשמעותית של דלדול רילין בנוירונים מסוימים ואת התפקיד המגן של אסטרוציטים עם ביטויי גנים ספציפיים.
חוקרים מ MIT ערכו מחקר מקיף בנושא אלצהיימר מחלה, ניתוח ביטוי גנים באזורי מוח שונים כדי להבין מדוע תאים ומעגלים ספציפיים פגיעים.
המחקר זיהה נוירונים בהיפוקמפוס ובקורטקס האנטורינאלי כרגישים במיוחד בשל ביטוי מופחת של החלבון Reelin, הקשור לירידה קוגניטיבית. בנוסף, החוקרים מצאו כי אסטרוציטים מקדמים חוסן קוגניטיבי באמצעות פעילות נוגדת חמצון ומטבוליזם של כולין.
עדויות חדשות לאופן שבו תאים ומעגלים ספציפיים הופכים לפגיעים במחלת אלצהיימר נחשפו במחקר של MIT שפורסם ב-24 ביולי ב- טֶבַע. המחקר בגישה הפתוחה מתמקד גם בגורמים אחרים שעשויים לעזור לאנשים מסוימים להראות עמידות בפני ירידה קוגניטיבית, אפילו על רקע סימנים ברורים של פתולוגיה של המחלה.
כדי להדגיש יעדים פוטנציאליים להתערבויות לשמירה על קוגניציה וזיכרון, המחברים עסקו בהשוואה חדשה של ביטוי גנים על פני אזורי מוח מרובים באנשים עם או בלי מחלת אלצהיימר, וערכו ניסויי מעבדה כדי לבדוק ולאמת את הממצאים העיקריים שלהם.
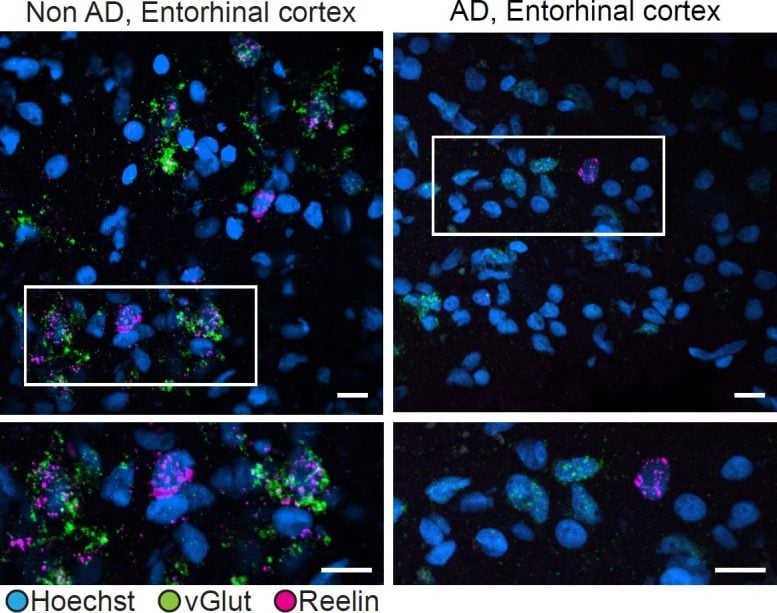
חוקרים השוו ביטוי של רילין בנוירונים מעוררים בקליפת המוח האנטורינאלית של אנשים עם (ימין) או בלי (שמאל) מחלת אלצהיימר. אצל אנשים ללא המחלה, vGlut (ירוק), סמן של נוירונים מעוררים, ורילין (מגנטה) באו לעתים קרובות לידי ביטוי יחד. אצל אנשים עם אלצהיימר, תאים מעוררים הפגינו הרבה פחות ביטוי של רילין. קרדיט: Tsai Lab/ MIT Picower Institute
דפוסי ביטוי גנים והבדלים תאיים באלצהיימר
לכל תאי המוח יש אותו דבר DNA אבל מה שגורם להם להיות שונים, הן בזהותם והן בפעילותם, הם הדפוסים שלהם של האופן שבו הם מבטאים את הגנים האלה. הניתוח החדש מדדה הבדלי ביטוי גנים ביותר מ-1.3 מיליון תאים של יותר מ-70 סוגי תאים בשישה אזורי מוח מ-48 תורמי רקמה, 26 מתוכם מתו עם אבחנה של אלצהיימר ו-22 מהם ללא. ככזה, המחקר מספק תיאור ייחודי גדול, מרחיק טווח ועם זאת מפורט כיצד פעילות תאי המוח שונה במחלת אלצהיימר לפי סוג תאים, לפי אזור מוח, לפי פתולוגיה של המחלה ולפי ההערכה הקוגניטיבית של כל אדם בעודו בחיים.
"אזורי מוח ספציפיים פגיעים באלצהיימר וישנו צורך חשוב להבין כיצד אזורים אלו או סוגי תאים מסוימים פגיעים", אומר שותף בכיר בסופר לי-הוי צאי, פרופסור למדעי המוח של פיקוור ומנהל מכון פיקוור ללמידה ו זיכרון ויוזמת המוח המזדקן ב-MIT. "והמוח הוא לא רק נוירונים. זה סוגים רבים אחרים של תאים. איך סוגי התאים האלה עשויים להגיב אחרת, תלוי איפה הם נמצאים, זה משהו מרתק שאנחנו רק בתחילת ההסתכלות עליו."
טכניקות מתקדמות בחקר אלצהיימר
מחבר בכיר מנוליס קליס, פרופסור למדעי המחשב וראש קבוצת הביולוגיה החישובית של MIT, משווה את הטכניקה המשמשת למדידת השוואות ביטוי גנים, תא בודד RNA פרופיל, להיות "מיקרוסקופ" מתקדם הרבה יותר מאלה שאפשרו לראשונה לאלואיס אלצהיימר לאפיין את הפתולוגיה של המחלה לפני יותר ממאה שנה.
"במקום שבו אלצהיימר ראה במיקרוסקופ שלו רובדי חלבון עמילואיד וסבך טאו מזורחן, ה'מיקרוסקופ' החד-תאי שלנו מספר לנו, תא אחר תא וגן אחר גן, על אלפי שינויים ביולוגיים עדינים אך חשובים בתגובה לפתולוגיה", אומר קליס. "חיבור המידע הזה למצב הקוגניטיבי של המטופלים חושף כיצד תגובות סלולריות קשורות לאובדן קוגניטיבי או חוסן, ויכול לעזור להציע דרכים חדשות לטיפול באובדן קוגניטיבי. הפתולוגיה יכולה להקדים תסמינים קוגניטיביים בעשור או שניים לפני שירידה קוגניטיבית מאובחנת. אם אין הרבה מה לעשות בקשר לפתולוגיה באותו שלב, נוכל לפחות לנסות להגן על המסלולים התאיים ששומרים על תפקוד קוגניטיבי".
Hansruedi Mathys, פוסט דוקטורט לשעבר ב-MIT במעבדת Tsai שכיום הוא עוזר פרופסור באוניברסיטת פיטסבורג; Carles Boix PhD '22, סטודנט לתואר שני לשעבר במעבדה של קליס, שהוא כעת פוסט דוקטורט בבית הספר לרפואה של הרווארד; ו-Leyla Akay, סטודנטית לתואר שני במעבדה של Tsai, הובילה את המחקר שניתח את קליפת המוח הקדם-מצחית, הקורטקס האנטורינאלי, ההיפוקמפוס, התלמוס הקדמי, הג'ירוס הזוויתי וקליפת המוח האמצע-טמפורלית. דגימות המוח הגיעו ממחקר הסדר הדתי ומפרויקט הזיכרון וההזדקנות של Rush באוניברסיטת Rush.
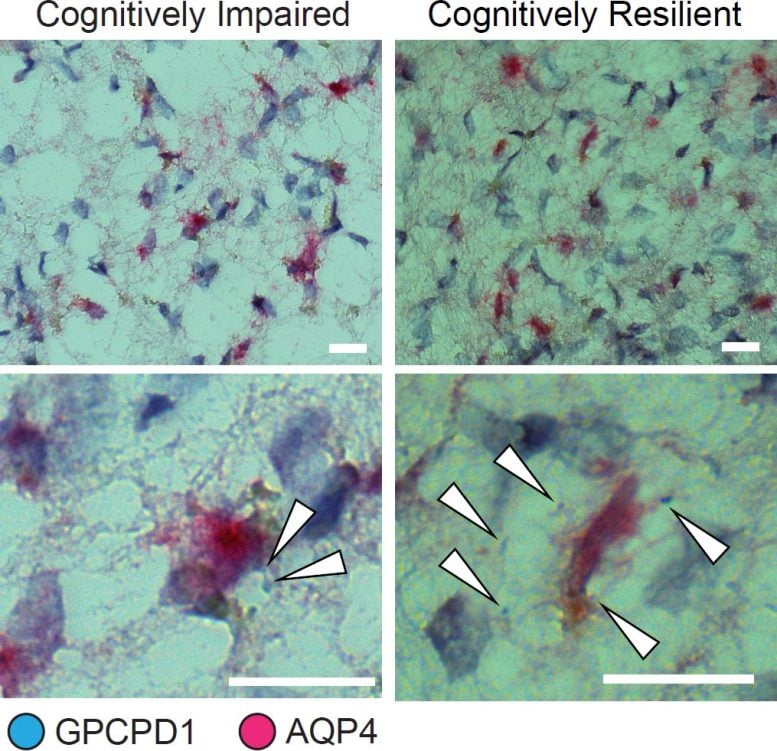
ביטוי של הגן GPCPD1 בתאי אסטרוציטים קשור לחוסן קוגניטיבי אצל אנשים עם פתולוגיה של אלצהיימר. כאן חיצים לבנים מציינים מקרים של ביטוי GPCPD1 (כחול) בתאי אסטרוציטים (מסומנים על ידי צביעה AQP4 במגנטה). יש הרבה יותר ביטוי ברקמה מהאדם החוסן קוגניטיבית (מימין). קרדיט: Tsai Lab/MIT Picower Institute
פגיעות עצבית ורילין
חלק מהסימנים המוקדמים ביותר לפתולוגיה עמילואידית ואובדן נוירונים באלצהיימר מתרחשים באזורים ממוקדי זיכרון הנקראים ההיפוקמפוס והקורטקס האנטורינאלי. באזורים אלה, ובחלקים אחרים של קליפת המוח, החוקרים הצליחו לאתר סיבה אפשרית לכך. סוג אחד של נוירון מעורר בהיפוקמפוס וארבעה בקליפת המוח האנטורינאלית נמצאו פחות משמעותית באנשים עם אלצהיימר מאשר באנשים ללא. אנשים עם דלדול של תאים אלה הצליחו בצורה גרועה משמעותית בהערכות קוגניטיביות. יתר על כן, נוירונים פגיעים רבים היו מחוברים זה לזה במעגל נוירוני משותף. וחשוב לא פחות, כמה ביטאו ישירות חלבון בשם Reelin, או שהושפעו ישירות מאותות Reelin. בסך הכל, לפיכך, הממצאים מדגישים באופן מובהק נוירונים פגיעים במיוחד, שאובדנם קשור לקוגניציה מופחתת, החולקים מעגל נוירוני ומסלול מולקולרי.
צאי מציין שרלין הפך לבולט בחקר האלצהיימר בגלל מחקר שנערך לאחרונה על גבר בקולומביה. הייתה לו מוטציה נדירה בגן Reelin שגרמה לחלבון להיות פעיל יותר, והצליח להישאר בריא מבחינה קוגניטיבית בגיל מתקדם למרות שיש לו נטייה משפחתית חזקה לאלצהיימר מוקדם. המחקר החדש מראה כי אובדן של נוירונים המייצרים רילין קשור לירידה קוגניטיבית. יחד, זה עשוי לומר שהמוח מרוויח מרלין, אבל נוירונים שמייצרים אותו עשויים ללכת לאיבוד לפחות אצל חלק מחולי אלצהיימר.
"אנחנו יכולים לחשוב על Reelin כבעל אולי איזושהי השפעה מגנה או מועילה", אומר אקאי. "אבל אנחנו עדיין לא יודעים מה זה עושה או איך זה יכול להעניק חוסן."
בניתוח נוסף, החוקרים מצאו גם שתת-סוגי נוירונים מעכבים פגיעים במיוחד שזוהו במחקר קודם מקבוצה זו בקליפת המוח הקדם-מצחית היו מעורבים גם באיתות רילין, מה שמחזק עוד יותר את המשמעות של המולקולה ומסלול האיתות שלה.
כדי לבדוק עוד יותר את התוצאות שלהם, הצוות בחן ישירות את דגימות רקמת המוח האנושי ואת המוח של שני סוגים של עכברים מודלים של אלצהיימר. אין ספק, הניסויים הללו הראו גם הפחתה של נוירונים חיוביים לרילין בקליפת המוח האנטורינאלית של האדם והעכבר.
גורמי חוסן ושימור קוגניטיבי
כדי למצוא גורמים שעשויים לשמר את הקוגניציה, אפילו בתוך הפתולוגיה, הצוות בדק אילו גנים, באילו תאים ובאילו אזורים, קשורים באופן הדוק ביותר לחוסן קוגניטיבי, שאותו הגדירו כתפקוד קוגניטיבי שיורי, מעל האובדן הקוגניטיבי האופייני הצפוי בהינתן הפתולוגיה הנצפית.
הניתוח שלהם הניב תשובה מפתיעה וספציפית: על פני מספר אזורי מוח, אסטרוציטים המבטאים גנים הקשורים לפעילות נוגדת חמצון ולמטבוליזם של כולין וביוסינתזה של פוליאמינים היו קשורים באופן משמעותי לקוגניציה מתמשכת, אפילו על רקע רמות גבוהות של טאו ועמילואיד. התוצאות חיזקו ממצאי מחקר קודמים בראשות צאי וסוזן לונדקוויסט, שבהם הראו שתוסף תזונה של כולין עזר לאסטרוציטים להתמודד עם חוסר ויסות של שומנים הנגרם על ידי הגן המשמעותי ביותר לסיכון לאלצהיימר, וריאנט APOE4. ממצאי נוגדי החמצון הצביעו גם על מולקולה שניתן למצוא כתוסף תזונה, spermidine, אשר עשויה להיות בעלת תכונות אנטי דלקתיות, אם כי קשר כזה ידרוש עבודה נוספת כדי לבסס את הסיבתיות.
כמו קודם, הצוות חרג מהתחזיות מניתוח ביטוי RNA חד-תא כדי לבצע תצפיות ישירות ברקמת המוח של דגימות. אלה שהגיעו מאנשים בעלי גמישות קוגניטיבית אכן הראו ביטוי מוגבר של כמה מהגנים המבוטאים אסטרוציטים שנחזית להיות קשורים לחוסן קוגניטיבי.
שיטה אנליטית חדשה ומערך נתונים ציבורי
כדי לנתח את הררי הנתונים של תא בודד, החוקרים פיתחו מתודולוגיה חזקה חדשה המבוססת על קבוצות של גנים המבוטאים בקואורדינטציה (הידועים כ"מודולי גנים"), ובכך ניצלו את דפוסי מתאם הביטוי בין גנים הקשורים פונקציונלית באותו מודול.
"באופן עקרוני, 1.3 מיליון התאים שסקרנו יכולים להשתמש ב-20,000 הגנים שלהם במספר אסטרונומי של שילובים שונים", מסביר קליס. "עם זאת, בפועל, אנו רואים תת-קבוצה קטנה בהרבה של שינויים מתואמים. זיהוי הדפוסים המתואמים הללו מאפשר לנו להסיק שינויים חזקים הרבה יותר, מכיוון שהם מבוססים על מספר גנים באותו מודול מקושר תפקודית".
הוא הציע אנלוגיה זו: עם מפרקים רבים בגופם, אנשים יכולים לנוע בכל מיני דרכים מטורפות, אבל בפועל הם עוסקים בהרבה פחות תנועות מתואמות כמו הליכה, ריצה או ריקוד. השיטה החדשה מאפשרת למדענים לזהות תוכניות ביטוי גנים מתואמות כאלה כקבוצה.
בעוד שהמעבדות של קליס וצאי כבר דיווחו על כמה ממצאים ראויים לציון ממערך הנתונים, החוקרים מצפים שעוד תגליות רבות, אולי משמעותיות, עדיין ממתינות להימצא בהמון הנתונים. כדי להקל על גילוי כזה, הצוות פרסם כלי ניתוח והדמיה שימושיים יחד עם הנתונים באתר האינטרנט של קליס.
"מערך הנתונים הוא כל כך עשיר. התמקדנו רק בכמה היבטים בולטים שלדעתנו הם מאוד מאוד מעניינים, אבל בשום אופן לא מיצינו את מה שניתן ללמוד עם מערך הנתונים הזה", אומר קליס. "אנחנו מצפים לעוד תגליות רבות קדימה, ואנו מקווים שחוקרים צעירים (בכל הגילאים) יצללו פנימה ויפתיעו אותנו בעוד הרבה תובנות".
בהמשך, אומר קליס, החוקרים חוקרים את מעגלי הבקרה הקשורים לגנים המובעים בצורה דיפרנציאלית, כדי להבין את הווריאציות הגנטיות, הרגולטורים וגורמי מניע אחרים שניתן לשנות כדי להפוך את מעגלי המחלה על פני אזורי מוח, סוגי תאים ושונים. שלבי המחלה.
מחברים נוספים של המחקר כוללים את Ziting Xia, Jose Davila Velderrain, Ayesha P. Ng, Xueqiao Jiang, Ghada Abdelhady, Kyriaki Galani, Julio Mantero, Neil Band, Benjamin T. James, Sudhagar Babu, Fabiola Galiana-Melendez, Kate Louderback, Dmitry פרוקופנקו, רודולף א' טנזי ודיוויד א' בנט.
התמיכה במחקר הגיעה מה- המכונים הלאומיים לבריאותמכון Picower ללמידה וזיכרון, קרן JPB, קרן ריפוי אלצהיימר, קרן משפחת רוברט א. ורנה אי. בלפר, אדוארדו יונרקיאן וג'וזף דיסאבאטו.

